La forme, ça compte ! Comprendre les vaccins à verrou moléculaire
La plupart d’entre nous ne réfléchissent pas particulièrement à la manière dont un vaccin est fabriqué. En général, nous pensons au rendez-vous pris pour se faire vacciner, à l'aiguille, voire au bras endolori en fin de journée. Mais en fait, derrière tout cela, il y a des scientifiques qui planchent sur une question étonnamment délicate : pour mettre au point un vaccin plus efficace, comment montrer au système immunitaire à quoi ressemble vraiment un virus ?
C’est-là un point qui a plus d’importance qu'on ne le réalise généralement. Prenons le virus respiratoire syncytial (VRS). La majorité des infections par le VRS ressemblent à un rhume ordinaire. Mais à l'échelle mondiale, le VRS déclenche chaque année 33 millions d'infections respiratoires sévères chez les jeunes enfants, dont 95 % concernant des pays à revenus faibles ou intermédiaires. Et chez la personne âgée, le VRS est de plus en plus reconnu comme une cause sérieuse d'hospitalisation, avec un degré de sévérité parfois équivalent à celui de la grippe au sein des populations vulnérables.
Pour Keith Chappell, conseiller scientifique chez Sanofi, ce problème a mis en lumière un défi qu'il cherche à résoudre depuis plus d'une décennie : comment viser une cible mouvante ?
La conception des vaccins et le problème des protéines virales instables
Le système immunitaire ne reconnaît pas un virus par son nom. Il le reconnaît à sa forme. À la surface de chaque virus, on trouve des protéines qui agissent comme de minuscules grappins, indispensables à l'invasion. Lorsqu'un virus se lie à une cellule, ces protéines se transforment et changent de forme, ce qui permet au virus de fusionner avec la cellule, de la pénétrer et de démarrer l'infection.
Pour qu'un vaccin soit efficace, il doit montrer au système immunitaire de quoi ont l’air ces protéines avant leur changement de forme — ce que les chercheurs appellent la forme « pré-fusionnelle » de la protéine. S’il apprend à reconnaître cette forme pré-fusionnelle du VRS, le système immunitaire peut essayer de stopper le virus avant l'infection.
C'est ici que débute le défi de la mise au point d’un vaccin.
Les protéines virales susceptibles d’apporter la meilleure protection contre l'infection par le VRS sont aussi les moins stables. Dans la nature, ces protéines sont dans un état tendu et fragile, à l’instar d’un ressort comprimé sous tension. Mais une fois que les chercheurs les extraient du virus pour les produire en laboratoire et comme on pouvait s’y attendre, les protéines se détendent et prennent adoptent une forme différente, plus relâchée.
Or, c'est précisément à ce moment que les chercheurs, qui veulent se servir de ces délicates protéines pour entraîner le système immunitaire, ont besoin qu'elles restent sous tension.
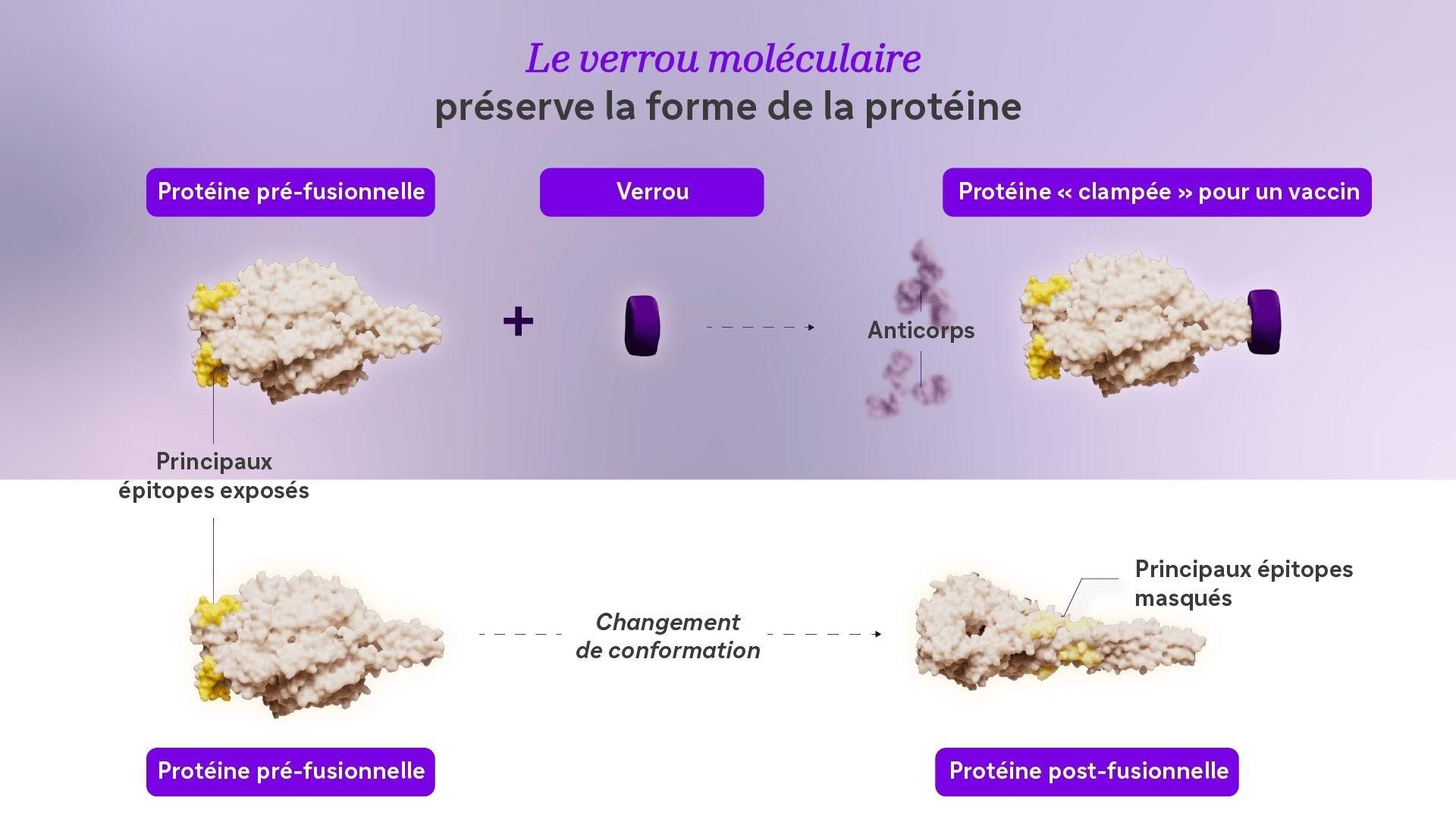
Figure 2. Le verrou moléculaire préserve la forme de la protéine. Lorsqu'un verrou moléculaire (violet) est utilisé, la protéine F du VRS reste dans sa conformation pré-fusionnelle (en haut). Le verrou moléculaire permet aux épitopes clés de la protéine, en jaune, de rester accessibles au système immunitaire et à la production d'anticorps. La protéine F du VRS subit un changement de forme sans verrou moléculaire (en bas).
« Du fait de ce changement de forme, il est très difficile de fabriquer isolément les protéines lorsqu’elles sont dans l’état instable qui doit être le leur », explique Keith. Au moment où les protéines sont purifiées et formulées en vue de la fabrication du vaccin, il est possible qu’elles n’aient plus l’aspect que le système immunitaire doit pouvoir reconnaître comme constituant une menace infectieuse. Il est possible qu’il réagisse tout de même, mais sans aller jusqu’à fabriquer les anticorps les plus protecteurs, ceux capables de bloquer l'infection dès sa première étape.
Alors, comment maintenir une protéine dans une forme qu'elle cherche spontanément à quitter ?
Une leçon tirée de l'infection naturelle : cibler la forme pré-fusionnelle de la protéine virale
Les premiers éléments de réponse à cette question sont venus d’une constatation faite par l'équipe de Keith au début de sa carrière. Lorsqu’un patient se rétablissait d'une infection naturelle au VRS, son organisme fabriquait de puissants anticorps neutralisants. Mais ces anticorps ne ciblaient pas le virus une fois entré dans la cellule et ne visaient que la protéine virale avant qu'elle ne change de forme pour pénétrer la cellule.
Cette observation a profondément modifié les données du problème : il fallait avant tout viser la structure pré-fusionnelle. Si les anticorps reconnaissaient la forme pré-fusionnelle de la protéine, le vaccin devait présenter exactement cette structure. Restait le problème de la stabilité. Comment maintenir les protéines vaccinales dans leur forme pré-fusionnelle assez longtemps pour que le système immunitaire apprenne à les reconnaître ?
La structure du verrou moléculaire : une configuration empruntée à la nature
Plutôt que de reprendre le procédé à zéro pour fabriquer des protéines différentes, Keith et les membres de son équipe ont choisi d’emprunter un concept de stabilité trouvé dans la nature.
C’est ainsi qu’ils ont ont créé un « verrou moléculaire », petit échafaudage synthétique qui maintient les protéines virales dans leur forme pré-fusionnelle instable. Grâce à ce verrou, au moment où le vaccin pénètre l'organisme, le système immunitaire repère le virus dans sa forme la plus susceptible de favoriser de solides réponses immunitaires.
C’est un phénomène que Keith décrit souvent par une image simple : dans un bouquet de fleurs, on peut comparer les fleurs aux protéines virales. Le verrou, c'est la main qui tient le bouquet. Sans la main, tout l'arrangement s'effondre.
Ces travaux scientifiques ont mené à la fondation en 2018 de Vicebio, une biotech dédiée au développement de la technologie du verrou moléculaire. Cette société fait désormais partie intégrante de Sanofi.
Début 2020, la plateforme a connu son premier test en conditions réelles.
La technologie vaccinale à l'épreuve d'une crise mondiale
Alors que la COVID-19 se répandait dans le monde entier, les chercheurs se sont rapidement mis au travail pour appliquer l'approche du verrou moléculaire à un candidat vaccin contre le SARS-CoV-2. Le degré d’urgence était sans précédent. Les laboratoires du monde entier faisaient tout ce qui était en leur pouvoir pour mettre au point des vaccins contre un virus qui avait paralysé des pays entiers.
Le programme a avancé jusqu'aux essais cliniques. Le vaccin semblait sûr. Il avait engendré une réponse immunitaire. Puis une complication est survenue.
La conception initiale du verrou moléculaire utilisait un élément structural emprunté à une protéine du VIH. Scientifiquement, le choix était judicieux ; la protéine du VIH apportait une excellente stabilité et ne présentait aucun risque d'infection. Mais chez certains patients de l'essai, elle a déclenché la fabrication d’anticorps interférant avec certains tests diagnostiques du VIH avec un risque de faux positifs. Ce fut la fin programme… « Vite commencé, vite fini », se souvient Keith. « Mais nous avions beaucoup appris !»
Pour Keith, ce revers avait renforcé une conviction qu’il avait toujours eue.
Derrière chaque vaccin, on trouve des gens qui ont consacré leur carrière à protéger des familles et à prévenir les maladies graves

Keith Chappell
Conseiller scientifique
Plutôt que d'abandonner la plateforme, l'équipe a choisi de la repenser. Un verrou de deuxième génération est venu remplacer l'élément dérivé du VIH par un domaine de stabilisation différent, ce qui a permis de préserver les avantages structuraux tout en éliminant les interférences diagnostiques. C’est ainsi que ce qui avait commencé par un échec a finalement débouché sur une véritable leçon d'ingénierie. La plateforme en est ressortie encore plus solide.
Avec l'acquisition de Vicebio par Sanofi, l'objectif est de porter ce travail sur une scène mondiale plus large, en associant l'innovation scientifique à l'expérience de la fabrication vaccinale à grande échelle.
Un processus de fabrication familier, conçu pour la rapidité
Une fois résolu le problème de la forme, on n’avait cependant fait que la moitié du chemin. Le verrou moléculaire devait également être pratique et permettre une fabrication en série.
Mais il s’avère que son processus de fabrication est similaire aux méthodes déjà utilisées pour produire d'autres médicaments biologiques, comme les anticorps thérapeutiques. Les fabricants de vaccins sont donc en mesure d'utiliser les infrastructures existantes, plutôt que d’avoir à construire de nouvelles installations spécialisées, ce qui allait permettre une production à grande échelle fiable.
En fait, le véritable avantage réside dans la notion de rapidité. Étant donné que structure du verrou reste la même d'un vaccin à l'autre, il suffit de modifier la séquence génétique de la protéine virale cible. Une fois que le génome d'un pathogène est connu — ce qui peut se produire en quelques jours après l'identification d'une nouvelle menace virale — les chercheurs peuvent concevoir de nouveaux candidats vaccins et passer rapidement aux tests.
Cette approche plug and play est particulièrement intéressante pour la préparation aux pandémies. Face à un nouveau foyer viral, le fait de pouvoir adapter rapidement une technologie vaccinale existante pourrait considérablement réduire les délais de développement. Plutôt que de reprendre à zéro la conception du vaccin, les chercheurs pourraient intégrer la séquence génétique du nouveau pathogène et tirer parti d’un processus de fabrication validé.
Cette possibilité vient renforcer la biosécurité mondiale en réduisant la fenêtre de temps entre l'identification d'un pathogène et la livraison d'un vaccin et en faisant gagner un temps précieux lors d’une crise où chaque jour compte.
La logistique a aussi son importance. Les vaccins protéiques avec verrou moléculaire peuvent survivre dans des conditions de réfrigération standard (4 °C), ce qui simplifie transport et stockage, notamment là où il est difficile voire impossible de maintenir des températures très basses. Les vaccins peuvent ainsi profiter à un plus grand nombre de patients dans le monde.
Les vaccins combinés : vers une protection simplifiée
La technologie du verrou moléculaire permet également des vaccins combinés, avec une seule injection qui protège contre plusieurs virus respiratoires. Les combinaisons de vaccins réduisent le nombre d’injections nécessaires, alors que des données fiables montrent qu’elles permettent de renforcer l’observance tout en faisant gagner du temps et en réduisant la complexité logistique. On peut ainsi faire bénéficier patients et systèmes de santé d’une meilleure prévention des maladies.
Un vaccin bivalent ciblant le VRS et le métapneumovirus humain (HMPV) est actuellement en cours d'évaluation, outre une formulation trivalente ciblant le VRS, le HMPV et le virus para-influenza (PIV3). Combiner plusieurs protéines virales dans un seul vaccin est scientifiquement complexe ; chaque composant doit rester stable au sein de la même formulation sans interférer avec les autres. Mais cela devient possible quand on part de protéines déjà stabilisées grâce à un verrou moléculaire.

Figure 3. Différentes protéines avec leurs verrous moléculaires. Ces protéines peuvent être utilisées en combinaisons variées pour produire de nouveaux vaccins ciblant plusieurs menaces infectieuses.
À terme, les vaccins combinés pourraient concerner la grippe ou la COVID-19, offrant potentiellement une large protection respiratoire grâce à une seule et unique vaccination annuelle. L'objectif à long terme consiste à simplifier l’immunisation, en réduisant le nombre de vaccins nécessaires, tout en maintenant voire en améliorant l'efficacité.
Keith insiste sur le fait que la technique du verrou moléculaire n'est pas destinée à se substituer à d'autres technologies vaccinales. « Je pense qu’il s’agit d’un véritable complément », dit-il. « Chaque plateforme a ses avantages et ses inconvénients. » Chaque virus, chaque population et chaque contexte peuvent nécessiter des approches différentes. Élargir la gamme d'outils mis à la disposition des chercheurs renforce notre capacité à répondre à des défis sanitaires en constante évolution.
La technologie du verrou moléculaire a commencé par une idée simple : la forme a son importance, et le système immunitaire doit savoir reconnaitre la bonne. Si elle tient ses promesses, elle se traduira non seulement par un progrès scientifique, mais aussi par une réduction du nombre d'hospitalisations et par une augmentation du nombre de vies humaines discrètement protégées contre les maladies graves.
Page mise à jour en avril 2026