À la une
26 janvier 2026
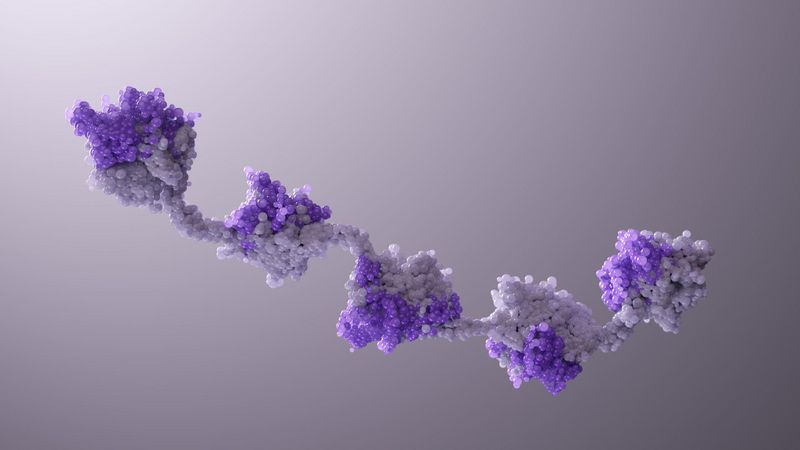
1, 2, 3 cibles ? Jusqu’à 5 sous-unités différentes de Nanobody® : vers un nouveau médicament ?
20 avril 2026
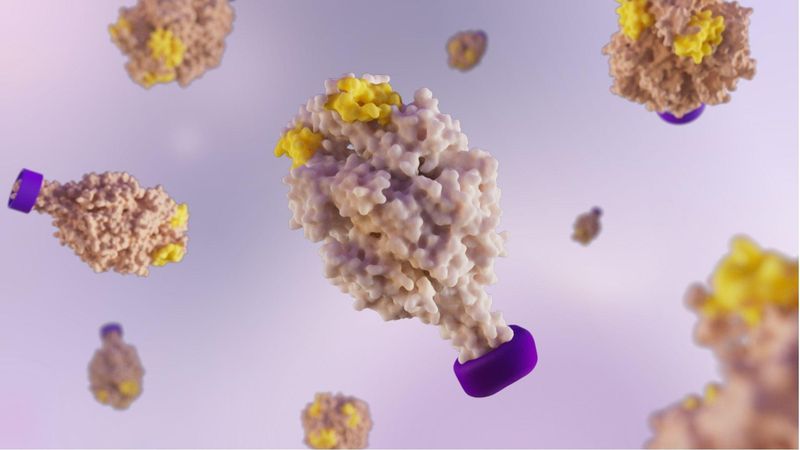
La forme, ça compte ! Comprendre les vaccins à verrou moléculaire

3 avril 2026
La voie rapide (et intense) : l’approbation accélérée, plus loin et plus vite pour les patients
L'IA et la recherche

24 février 2026
L'IA à chaque étape de la chaîne de valeur R&D : la prise de décisions concernant le portefeuille

13 janvier 2026
L'IA à chaque étape de la chaîne de valeur de la R&D : Fabrication - Laboratoires numériques et outils à apprentissage continu

4 septembre 2025
L'IA à travers la chaîne de valeur R&D : le développement clinique

9 juillet 2025
L’IA à chaque étape de la chaîne de valeur R&D: découverte de médicaments
Tout sur Notre Science
Année
20 mai 2026
Des études cliniques à l’image de la vraie vie
20 mai 2026
Au-delà des études cliniques : il est important d’écouter
20 avril 2026
La forme, ça compte ! Comprendre les vaccins à verrou moléculaire
3 avril 2026
La voie rapide (et intense) : l’approbation accélérée, plus loin et plus vite pour les patients
30 mars 2026
Making it Real : transformer les avancées de la science en réalité pour les patients
26 janvier 2026
1, 2, 3 cibles ? Jusqu’à 5 sous-unités différentes de Nanobody® : vers un nouveau médicament ?
6 janvier 2026
Notre approche humaine en matière de partenariats dans le contexte changeant de la biotechnologie
7 novembre 2025
Respiration des patients : Répondre aux besoins non satisfaits des patients en santé respiratoire
19 septembre 2025
